محققان آزمایشگاه جکسون (JAX)، مؤسسه Broad از MIT و دانشگاه هاروارد و دانشگاه ییل با استفاده از هوش مصنوعی (AI) به دستاوردی بزرگ در کنترل ژنها دست یافتهاند.
این رویکرد نوآورانه از هوش مصنوعی برای طراحی سوئیچهای مصنوعی DNA به نام عناصر سیستنظیمی (CREs) استفاده میکند که میتوانند فعالیت ژنها را بهطور دقیق در بافتها یا انواع خاصی از سلولها تنظیم کنند.
ابزاری دقیق برای کنترل ژنها
یکی از چالشهای اصلی در مهندسی ژنتیک، توانایی کنترل این است که ژنها کجا و چه زمانی در موجودات زنده فعال شوند. در حالیکه فناوریهای ویرایش ژن مانند CRISPR کار اصلاح ژنها را آسانتر کردهاند، اطمینان از اینکه این تغییرات فقط بر بافتها یا سلولهای مورد نظر تأثیر بگذارد، همچنان دشوار است.
تیم تحقیقاتی مسئول این مطالعه در تلاش برای حل این مسئله، به طراحی توالیهای مصنوعی DNA پرداختند که بهعنوان سوئیچهای دقیق برای روشن یا خاموش کردن بیان ژن عمل کرده و به این ترتیب کنترل بیشتری بر مداخلات ژنتیکی فراهم میکنند.
رایان تویی، یکی از نویسنده ارشد این مطالعه، میگوید:
آنچه این عناصر طراحیشده را خاص میکند، این است که آنها ویژگیهای فوقالعادهای نسبت به نوع سلول هدفی که برای آن طراحی شدهاند، دارند.
این روش این امکان را به ما میدهد که بیان یک ژن را تنها در یک بافت افزایش یا کاهش دهیم، بدون اینکه بر سایر قسمتهای بدن تأثیر بگذارد.
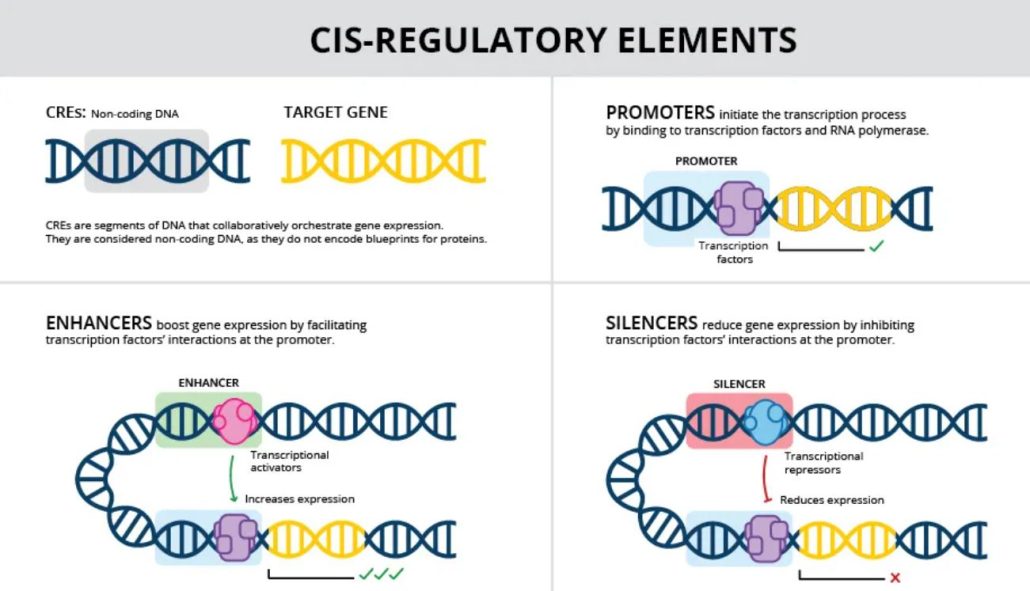
درک گرامر DNA در عناصر سیستنظیمی
هر سلول در بدن حاوی کد ژنتیکی یکسانی است، اما همه ژنها در هر سلول فعال نیستند. عناصر تنظیمی DNA مانند عناصر سیستنظیمی بهعنوان سوئیچهای کنترلی عمل میکنند و اطمینان حاصل میکنند که ژنهای درست در سلولهای مناسب و در زمان مناسب فعال شوند. چالش اصلی، رمزگشایی از “گرامر” این توالیها بوده است؛ یعنی درک قوانین حاکم بر عملکرد آنها.
برای حل این مشکل، تیم از یادگیری عمیق، شاخهای از هوش مصنوعی، استفاده کرد تا مدلی طراحی کنند که قادر به پیشبینی فعالیت عناصر سیستنظیمی باشد. با تجزیه و تحلیل حجم عظیمی از دادههای DNA، مدل هوش مصنوعی توانست الگوهایی را کشف کند که تشخیص آنها برای انسان دشوار بود. این نتایج به محققان امکان داد تا بهتر بفهمند چگونه چیدمان توالیها در این عناصر بر فعالسازی ژن تأثیر میگذارد.
نتایج این مطالعه به محققان کمک کرد تا بهتر درک کنند که چگونه چیدمان توالیها در عناصر سیستنظیمی بر فعالسازی ژن تأثیر میگذارد و زمینه را برای طراحی عناصر سیستنظیمی مصنوعی با عملکردهای بسیار خاص فراهم کرد.
با استفاده از پلتفرمی به نام CODA (بهینهسازی محاسباتی فعالیت DNA)، محققان توانستند هزاران عنصر سیستنظیمی جدید طراحی کنند که میتوانند بیان ژن را در انواع خاصی از سلولها کنترل کنند.
آزمایش روی موجودات زنده
برای تأیید عملکرد CREهای طراحیشده با هوش مصنوعی، این تیم آزمایشهایی را روی مدلهای حیوانی از جمله ماهی زبرا و موش انجام داد. در یکی از آزمایشها، یک عنصر سیستنظیمی مصنوعی با دقت یک پروتئین فلورسانت را فقط در کبد ماهی زبرا فعال کرد که در هیچ قسمت دیگری از بدن فعال نشد.
این سطح از دقت میتواند در درمانهایی که نیاز به بیان ژنی در یک بافت خاص دارند، بدون تأثیر بر سایر بافتها، تحولی عظیم ایجاد کند.
با فراهم کردن کنترل بیشتر بر مکان و زمان فعالسازی ژنها، این عناصر سیستنظیمی طراحیشده توسط هوش مصنوعی میتوانند در انواع کاربردهای درمانی استفاده شوند، از درمان بیماریهای ژنتیکی گرفته تا بهینهسازی بازسازی بافتها.
با تکامل این رویکرد مبتنی بر هوش مصنوعی برای طراحی عناصر سیستنظیمی، امکانات وسیعی پدیدار میشود. فراتر از تحقیقات پایه، این سوئیچهای مصنوعی DNA میتوانند در زیستساخت یا توسعه درمانهای پیشرفته برای طیف وسیعی از بیماریها استفاده شوند و راهکارهای موثرتری برای دستکاری ژنها با دقتی بیسابقه فراهم آورند.
رایان تویی در بیانیهای مطبوعاتی گفت:
این فناوری راه را برای نوشتن عناصر تنظیمی جدید با عملکردهای از پیش تعیینشده هموار میکند. چنین ابزارهایی نه تنها برای تحقیقات پایه ارزشمند خواهند بود، بلکه میتوانند پیامدهای مهمی در زمینه پزشکی بهویژه در کنترل بیان ژن در انواع خاصی از سلولها برای اهداف درمانی، داشته باشند.
این مطالعه بهتازگی در مجله Nature منتشر شده است.
منبع: Interestingengineering






![آپدیت HyperOS 3 باعث از کار افتادن گوشیهای شیائومی با رام جعلی میشود [راه حل رفع مشکل]](https://aero-tech.ir/wp-content/uploads/2026/01/9513-1-HyperOS-3-Update.jpg)