نانوقطرههای بینی که حامل اسیدهای نوکلئیک کروی (SNA) مبتنی بر طلا هستند، میتوانند به مغز نفوذ کرده و مسیرهای قدرتمند ایمنی را برای هدف قرار دادن گلیوبلاستوما فعال کنند. در موشها، این درمان تومورها را از بین برد و در صورت استفاده همراه با داروهای تقویتکننده سلولهای T، ایمنی طولانیمدت ایجاد کرد.
پیشرفت غیرتهاجمی نانوداروها برای سرطان مرگبار مغز
محققان دانشکده پزشکی دانشگاه واشنگتن در سنت لوئیس، با همکاری محققان دیگر در دانشگاه نورثوسترن، یک استراتژی غیرتهاجمی با هدف درمان یکی از خطرناکترین و سریعترین سرطانهای مغز ایجاد کردهاند. رویکرد آنها متکی بر ساختارهای نانومقیاس با مهندسی دقیق است که ترکیبات ضدتوموری قدرتمند را از طریق قطرههای ساده بینی مستقیماً به مغز میرسانند. در آزمایشهایی که روی موشها انجام شد، این روش تحویل با موفقیت گلیوبلاستوما را هدف قرار داد و دفاع ایمنی مغز را تقویت کرد، در حالیکه کمتر از بسیاری از درمانهای مشابهی که اکنون در حال بررسی هستند، تهاجمی بود.
این یافتهها ماه جاری میلادی در مجله PNAS منتشر شده است.
درک پیشرفت سریع و موانع درمان گلیوبلاستوما
گلیوبلاستوما از آستروسیتها (نوعی سلول مغزی) شروع میشود و شایعترین تومور مغزی بدخیم در ایالات متحده است که تقریباً از هر ۱۰۰,۰۰۰ نفر، سه نفر را تحت تأثیر قرار میدهد. این تومور به سرعت رشد میکند و تقریباً همیشه کشنده است. یکی از موانع اصلی درمان آن، دشواری انتقال ایمن داروهای درمانی به مغز است.
دکتر الکساندر اچ. استگ، استاد و نایب رئیس تحقیقات در گروه جراحی مغز و اعصاب خانواده تیلور در دانشگاه پزشکی واشنگتن و یکی از نویسندگان مسئول این مطالعه، میگوید:
ما میخواستیم این واقعیت را تغییر دهیم و یک درمان غیرتهاجمی ایجاد کنیم که پاسخ ایمنی را برای حمله به گلیوبلاستوما فعال کند.
استگ همچنین مدیر تحقیقات مرکز تومور مغزی در مرکز سرطان سیتمن است. او افزود:
با این تحقیق، ما نشان دادهایم که نانوساختارهای مهندسیشده دقیق، به نام اسیدهای نوکلئیک کروی (SNAs)، میتوانند با خیال راحت و به طور مؤثر، مسیرهای ایمنی قدرتمند را در مغز فعال کنند. این امر نحوه دستیابی به ایمونوتراپی سرطان را در تومورهایی که دسترسی به آنها دشوار است، بازتعریف میکند.
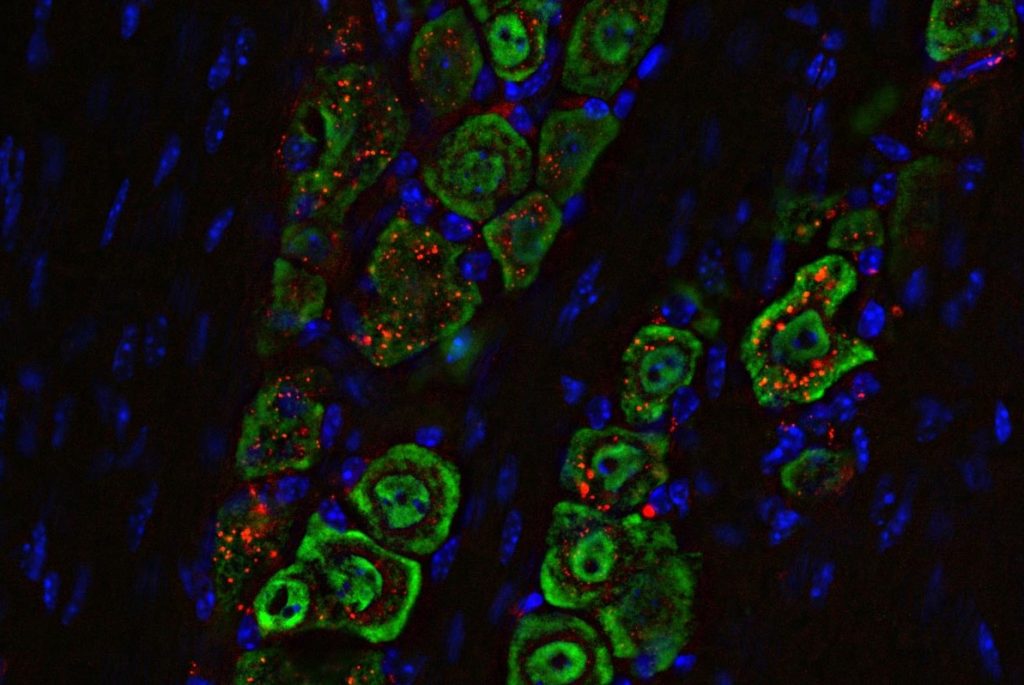
تبدیل “تومورهای سرد” به “گرم” با فعالسازی مسیر STING
تومورهای گلیوبلاستوما گاهی اوقات به عنوان “تومورهای سرد” توصیف میشوند، زیرا بهطور طبیعی یک واکنش ایمنی قوی را برانگیخته نمیکنند. این امر درمان آنها را نسبت به “تومورهای گرم” که پاسخ بهتری به ایمونوتراپیها میدهند، دشوارتر میکند. برای غلبه بر این مشکل، دانشمندان در حال بررسی راههایی برای فعال کردن یک مسیر سلولی به نام STING (مخفف محرک ژنهای اینترفرون) هستند. هنگامیکه یک سلول DNA خارجی را تشخیص میدهد، STING به راهاندازی پاسخ ایمنی کمک میکند.
تحقیقات قبلی نشان داده بود که داروهایی که برای فعالسازی STING طراحی شدهاند، میتوانند به آمادهسازی سیستم ایمنی برای شناسایی و حمله به گلیوبلاستوما کمک کنند. با این حال، این داروها به سرعت در بدن تخریب میشوند و تنها زمانی مؤثر عمل میکنند که مستقیماً به تومور تزریق شوند. دستیابی به دوزهای مکرر مورد نیاز برای مزایای پایدار، مستلزم اقدامات بسیار تهاجمی است.
دکتر آکانکشا ماهاجان، همکار تحقیقاتی فوقدکتری در آزمایشگاه استگ و نویسنده اول این مطالعه، میگوید:
ما واقعاً میخواستیم زمانیکه بیماران از قبل بیمار هستند، نیاز آنها به گذراندن این مراحل را به حداقل برسانیم و من فکر کردم که میتوانیم از پلتفرمهای اسید نوکلئیک کروی برای رساندن این داروها به روشی غیرتهاجمی استفاده کنیم.
اثربخشی انتقال از بینی به مغز در مدلهای موش
برای غلبه بر این مشکل، تیم استگ با دکتر چاد آ. میرکین، مدیر مؤسسه بینالمللی نانوتکنولوژی و استاد شیمی در دانشگاه نورثوسترن و یکی دیگر از نویسندگان مسئول، و تیم او همکاری کردند. میرکین اسیدهای نوکلئیک کروی را اختراع کرد؛ کلاس نانوساختارهایی که DNA یا RNA را به صورت متراکم در اطراف یک هسته نانوذره سازماندهی میکنند و او نشان داده است که آنها در مقایسه با روشهای تحویل استاندارد، قدرت درمانی بیشتری دارند. محققان دانشکده پزشکی واشنگتن و نورثوسترن، کلاس جدیدی از اسیدهای نوکلئیک کروی با هستههای طلا را ساختند که با قطعات کوتاهی از DNA برای تحریک فعالسازی مسیر STING در سلولهای ایمنی خاص پوشانده شدهاند. برای رساندن این داروها به مغز، تیم به بینی روی آورد.
درمان داخل بینی به عنوان یک روش تحویل بالقوه برای داروهایی که مغز را هدف قرار میدهند، مورد بررسی قرار گرفته است، اما هنوز هیچ درمان نانومقیاسی با استفاده از این روش برای فعال کردن پاسخهای ایمنی علیه سرطانهای مغز ایجاد نشده بود.
فعالسازی STING، ایمنی قوی ضد تومور را تحریک میکند
ماهاجان میگوید:
این اولین بار است که نشان داده میشود میتوانیم فعالسازی سلولهای ایمنی در تومورهای گلیوبلاستوما را زمانی که نانوداروها را از بینی به مغز میرسانیم، افزایش دهیم.
هدف تیم این بود که نشان دهند این رویکرد میتواند برای رساندن انتخابی دارو به مغز استفاده شود و پس از رسیدن به آنجا، بر روی سلولهای مناسب عمل خواهد کرد. برای هدف اول، آنها از یک برچسب مولکولی بر روی اسید نوکلئیک کروی استفاده کردند که در زیر نور مادون قرمز نزدیک قابل مشاهده بود. آنها دریافتند که نانودارو، هنگامی که به صورت قطراتی به مجاری بینی موشهای مبتلا به گلیوبلاستوما تزریق میشود، در امتداد مسیر عصب اصلی که عضلات صورت را به مغز متصل میکند، حرکت میکند. پاسخ ایمنی ایجاد شده توسط دارو در مغز، در سلولهای ایمنی خاص، به ویژه سلولهای موجود در خود تومور، متمرکز شد و پاسخهای مفیدی را در غدد لنفاوی ایجاد کرد. این دارو به سایر قسمتهای بدن که ممکن است عوارض جانبی ناخواستهای ایجاد کند، گسترش پیدا نکرد.
بررسی سلولهای ایمنی در داخل و نزدیک تومور نشان داد که این درمان با موفقیت مسیر STING را فعال کرده و سیستم ایمنی را برای مبارزه با تومور مسلح کرده است.
وعده بالینی و گامهای بعدی برای کاربرد
هنگامیکه این درمان جدید همراه با داروهایی که برای کمک به فعالسازی لنفوسیتهای T (نوع دیگری از سلولهای ایمنی) طراحی شدهاند، استفاده شد، تنها با یک یا دو دوز تومورها را ریشهکن کرد و ایمنی طولانیمدت در برابر عود آنها ایجاد کرد. در مجموع، نتایج بسیار بهتر از نتایج ایمونوتراپیهای فعالکننده STING فعلی بود.
استگ هشدار داد که فعالسازی مسیر STING به تنهایی، بدون تقویت از طریق سایر رویکردهای درمانی، قادر به درمان کامل گلیوبلاستوما نیست. فعال کردن مسیر STING به خودی خود برای مبارزه با گلیوبلاستوما کافی نیست، زیرا تومور راههای زیادی برای مسدود کردن یا خاموش کردن پاسخ ایمنی که STING برای فعالسازی آن در نظر گرفته شده، دارد. تیم او به دنبال اضافه کردن قابلیتهایی به نانوساختار خود هستند که سایر پاسخهای ایمنی را فعال کند. این امر میتواند به پزشکان اجازه دهد تا اهداف درمانی را دو یا سه برابر کرده و همه را در یک درمان واحد ترکیب کنند.
او میگوید:
این رویکردی است که امید به درمانهای ایمنتر و مؤثرتر برای گلیوبلاستوما و به طور بالقوه سایر سرطانهای مقاوم به درمانهای ایمنی را ارائه میدهد و گامی حیاتی به سوی کاربرد بالینی است.
منبع: Scitechdaily